- 首页
- 论文服务
- 科研支持
- 访学通
- 美捷登学院
Taqman探针法支原体检测试剂盒(UNG防污染版)GSDetect™ Taqman Mycoplasma Detection Kit (UNG plus)
GSDetect™ Taqman Mycoplasma Detection Kit(UNG plus)基于Taqman qPCR法,针对支原体16S rRNA的保守区域序列,设计特异性引物和荧光探针(FAM标记)用于支原体DNA的检测。本试剂盒可直接以细胞培养上清或血清等生物材料为模板,检测常见的16种支原体污染。
试剂盒内添加dUTP/UNG酶体系,能避免PCR产物气溶胶污染导致的假阳性,大幅提高检测的准确性。
产品特点
●操作简便,直接使用1μL细胞培养上清或血清进行检测,无需提取DNA。
●检测灵敏度高,准确率高,耐受青霉素和链霉素或其他抑制物的影响。
●特异性强,只能扩增支原体DNA,不会扩增细菌真菌或真核细胞的DNA。
●检测快速,最快1小时即可判定结果。
产品组分
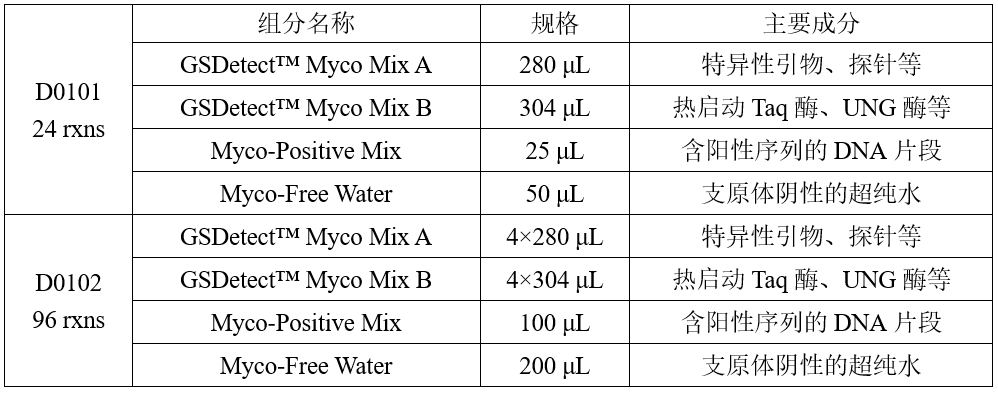
运输与保存
4℃运输,-20℃避光保存,保质期一年。
避免反复冻融,反复冻融次数不超过7次,短期使用时可在4℃保存一个月。
可检测的支原体类型

注意事项
1.使用前请仔细阅读本说明书。
2.规范检测操作,穿戴实验服、手套和口罩,并分区域进行反应体系的配置、样品处理与加样和PCR扩增,避免交叉污染。
检测流程
1.检测准备
1.1穿戴实验服、手套和口罩进行操作。
1.2规范检测操作,有条件的应分别在独立的制备区和扩增区进行操作。
1.3从试剂盒中取出各组分试剂,室温融化颠倒混匀,短暂离心后置于冰盒上备用。
2.反应体系配置
2.1根据待测样品数量配置如下反应体系:

2.2用移液器吹打混匀,并分装于八联管或96孔板中,每管吸取反应液24 μL。
2.3吸取1μL Myco-Free Water加入第一个反应管中,作为阴性对照。
2.4依次吸取1μL待测样品分别加入其余反应管中。
2.5吸取1μL Myco-Positive Mix加入最后一个反应管中,作为阳性对照。
注:步骤2.3至2.5应依次进行,即阳性对照必须最后一个加入。
3.PCR扩增(以ABI 7500设置为例)
3.1设置探针检测模式为Reporter: FAM,Quencher: NFQ-MGB,Passive reference: None。
3.2设置扩增循环条件如下:
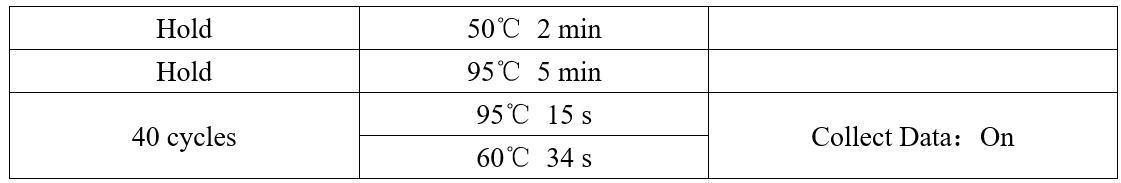
3.3反应结束后仪器自动保存结果,自动设置Threshold值和分析Ct值。也可根据实际情况手动设置,Start值可设为3~15,End值可设为5~20,在Log图谱窗口设置Threshold值,使阈值线位于扩增曲线指数期且阴性对照的扩增曲线平直或低于阈值线。
4.质量控制
4.1阳性对照:FAM检测通道有明显扩增曲线,Ct值<32。阴性对照:FAM检测通道无明显扩增曲线,Ct值≥40。
4.2不能同时满足4.1的质量控制要求时,应认定结果无效,检查反应体系和实验操作并排除污染等可能性后重新进行实验。
5.结果判定
5.1待测样品在FAM检测通道有明显扩增曲线,且Ct值<40,可判定待测样品为支原体阳性。
5.2对结果存疑或怀疑阴性对照有污染(如有扩增曲线或35<Ct值<40)时,可取2μL待测样品进行复检,并手动设置Threshold值和分析Ct值,后根据5.1判定复检结果。
- 上一篇:没有了
- 下一篇:没有了
- 返回栏目页
公司地址:武汉市江岸区中山大道岳飞街21号金源世界中心D座1201-1203室
Copyright © 2024 Medjaden All Rights Reserved. 版权所有 不得翻录
 鄂ICP备11002610号-1
鄂公网安备42010202000197
联系电话:027-85567377
鄂ICP备11002610号-1
鄂公网安备42010202000197
联系电话:027-85567377
联系人:陈经理 - 科研支持




 关注美捷登公众号
关注美捷登公众号
 美捷登公益直播
美捷登公益直播




