- 首页
- 论文服务
- 科研支持
- 访学通
- 美捷登学院
临床设计方案及注册指导临床试验注册属于科研及期刊出版规范中伦理学的范畴,国际期刊的审稿过程中往往实行一票否决制。根据美捷登的经验,很多作者并不清楚临床试验注册的必要性和相关途径,一些非常不错的临床试验往往在投稿过程中因为不符合临床试验报道的规范而被退稿。美捷登可以为您提供临床注册相关指导服务,有意者请联系我们。
在启动临床研究方案注册之前,研究者需要先准备好一份研究方案(如需要美捷登帮助指导准备研究方案,请查看“实/试验设计”),之后即可准备注册申请工作。
服务内容
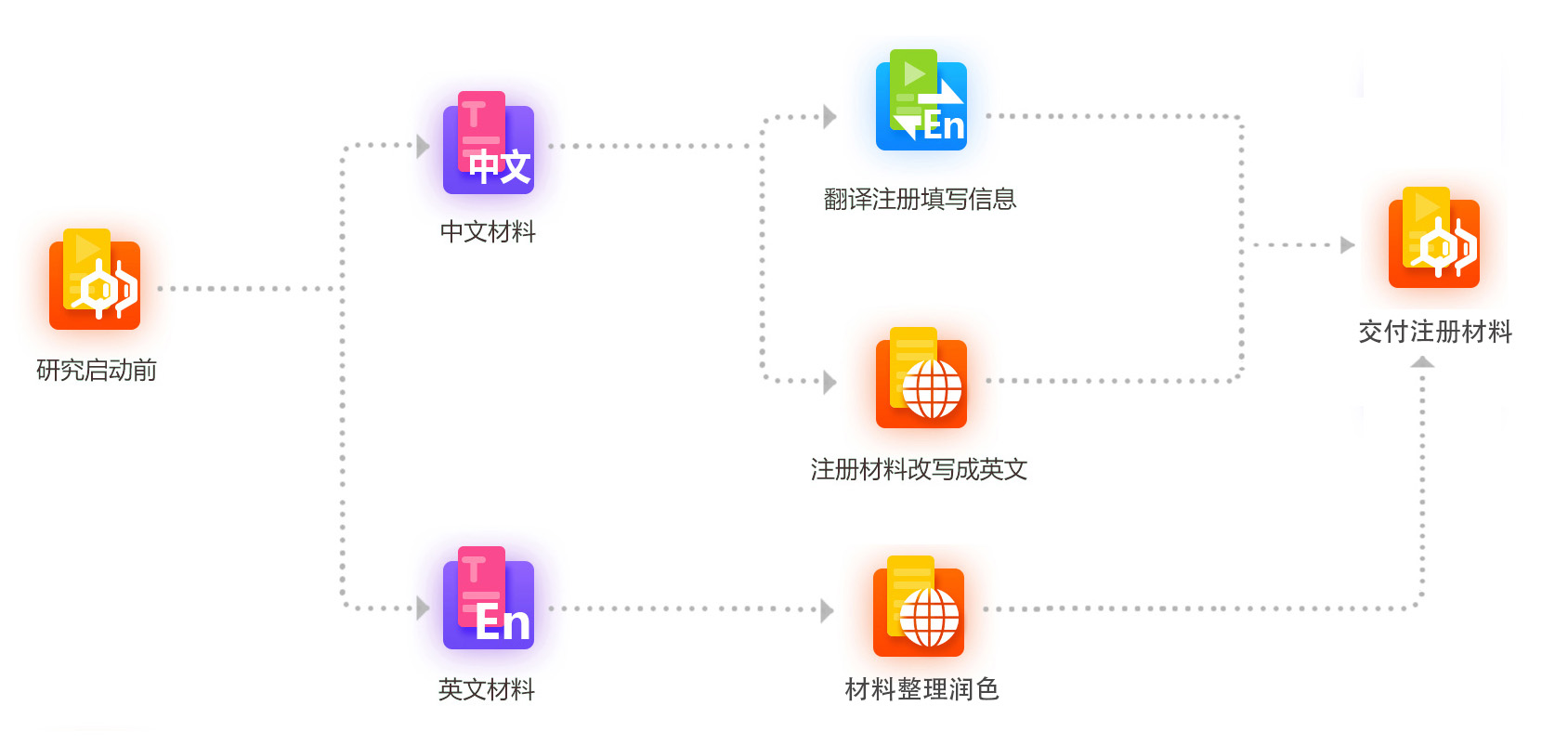
美捷登可提供以下二种临床试验注册指导帮助

临床试验注册中心(https://clinicaltrials.gov/),由美国国立卫生研究院组织其所属单位国立医学图书馆与美国食品药品监督管理局合作开发,注册语言为英文,只能在研究开始前注册。

中国临床试验注册中心(http://www.chictr.org.cn/)(中国,注册语言:中文)注册流程同上,与上述不同之处在于,此网站还可以在研究开始后补注册。
注册流程如下(从初步idea开始)
第一步:制作研究方案;
第二步:基于注册网站要求准备中/英文版本注册材料;
第三步:注册,需研究者配合提供相关材料;
第四步:数据定期更新/跟踪/维护。
以上环节美捷登均可提供指导服务,欢迎咨询。
投稿链接:https://online.medjaden.com
询价请联系客服:027-85567377
公司地址:武汉市江岸区中山大道岳飞街21号金源世界中心D座1201-1203室
Copyright © 2024 Medjaden All Rights Reserved. 版权所有 不得翻录
 鄂ICP备11002610号-1
鄂公网安备42010202000197
联系电话:027-85567377
鄂ICP备11002610号-1
鄂公网安备42010202000197
联系电话:027-85567377
联系人:陈经理 - 科研支持




 关注美捷登公众号
关注美捷登公众号
 美捷登公益直播
美捷登公益直播

